关于欧盟医疗器械术语EMDN的详尽介绍
奥斯曼提醒您重视查收!
EMDN的全称是European Medical Device Nomenclature,是欧盟委员会于2021年5月4日在CND的根底上发布的欧洲医疗器械定名系统。
根据MDR律例(EU)2017/745第26条和IVDR律例(EU)2017/746第23条,欧洲医疗器械定名法(EMDN)为欧洲医疗器械数据库(EUDAMED)供给撑持。
因为EMDN次要用于撑持MDR和IVDR的监管,因而它在MDR/IVDR设备文件和手艺文件、由通知布告机构停止的手艺文件取样、上市后监测、保镳和上市后数据阐发中也发扬着关键感化等。
它旨在撑持所有参与者在MDR/IVDR下的活动,并向患者供给关键设备阐明,包罗他们本身的设备以及市场上所有其他设备,并在EUDAMED注册。
EMDN的构造是如何的?
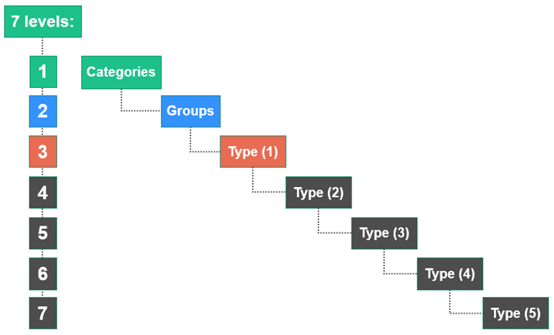
EMDN 的特征是其字母数字构造,成立在七级层级树中。它将医疗器械分为三个次要层级:
Categories类别:第一层级
Groups组:第二层级
Types类型:第三层级(需要时可扩展为几个更细的层级(1、2、3、4和5)
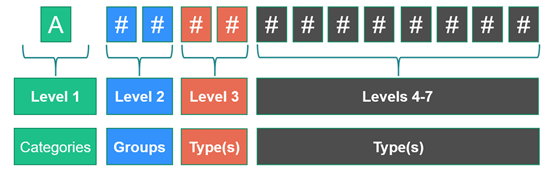
每个代码以一个大写英文字母开头,表达器械所属的“类别”,如W代表体外诊断器械。后面是两个数字,表达“组”和一系列数字,表达“类型”。更大位数设置为13。
展开全文
该若何获得EMDN 的拜候权限?
所有的利益相关者都能够免费利用整个EMDN。因而,造造商、患者、研究机构、从业人员、病院、药房等利益相关者都能够利用它。EMDN能够在webgate.ec.europa.eu/dy na2/emdn和欧盟委员会的MDCG文件网站上以pdf和excel格局拜候和下载。
注:欧盟委员会就欧洲医疗器械术语 (EMDN) 的英文版停止了为期一个月的在线征询,截行日期为 2021 年 6 月 4 日。其目标是搜集用户和广阔医疗保健界对任何翻译错误和语法定见的反应,在对所供给的定见停止处置后,EMDN的第二版将在2021年第三季度发布。
此外,医疗器械软件(J、W 和 Z 类)的新术语和描述也将会在第二版中推出。
EMDN的次要原则是什么?
EMDN基于欧盟委员会和欧盟监管机构配合造定的根本关键原则。那些原则包罗但不限于:
(a) 监管者主导:监管者在术语的治理、验证、更新和定见方面发扬着关键感化。
(b) 构造化:术语具有通明的条理构造.
(c) 可揣测的:构造和内容连结足够不变,以容许术语的各类监管用处,同时容许手艺立异。
(d) 通明:术语和描述的更新政策是合理的,
(e) 宽大性:按期审查对所有人开放.
(f) 可用:所有用户都能够利用完全的术语、阐明和代码。
(g) 无障碍:与其他运营商比拟,任何造造商或天然人/法人在利用术语方面都不该收取费用或遭受任何鄙视。
(h) 国际:在MDR/IVDR申请之日获得国际承认。
